¿Se puede pronosticar o prevenir la enfermedad de Parkinson?, es la pregunta recurrente de pacientes, familiares, cuidadores y la comunidad en general.
La respuesta clara y contundente es que todavía no hay forma de pronosticar o prevenir la enfermedad de Parkinson.
Sin embargo, de acuerdo con el médico mejicano, Carlos Muñoz Retana en su sitio web Geosalud, en la actualidad se adelantan varias investigaciones en ese sentido.
Dice el médico que los investigadores están buscando ahora un biomarcador -una anormalidad bioquímica que puedan compartir todos las personas diagnosticadas con Parkinson- que podría identificarse mediante técnicas de examen o por simple prueba química administrada a las personas que no tienen síntomas de Parkinson.
Precisa también que la exploración por tomografía de emisión de positrones (PET) puede conducir a adelantos importantes en nuestro conocimiento acerca de la enfermedad de Parkinson.
Las exploraciones por tomografía de emisión de positrones del cerebro producen fotos de los cambios químicos a medida que ocurren en el cerebro viviente.
Utilizando PET, los investigadores científicos pueden estudiar los receptores de dopamina del cerebro (los lugares en las células nerviosas que se unen a la dopamina) para determinar si la pérdida de actividad dopamínica sigue o precede a la degeneración de las neuronas que fabrican este producto químico.
Esta información podría ayudar a los científicos a comprender mejor el proceso de la enfermedad y conducir potencialmente a mejores tratamientos.
Investigaciones sobre factores ambientales y genéticos
En la última década, la investigación ha cimentado las bases para muchos de los nuevos y prometedores ensayos clínicos, tecnologías y tratamientos a base de medicamentos del presente.
La investigación de la enfermedad de Parkinson se concentra en muchas áreas. Algunos investigadores estudian las funciones y la anatomía del sistema motor y cómo éste regula el movimiento y está relacionado con los principales centros de mando en el cerebro.
Aunque el Parkinson no se hereda directamente, es posible que algunas personas sean más susceptibles o menos susceptibles genéticamente a contraerla. Por eso los científicos siguen estudiando los factores genéticos para determinar si uno o muchos genes defectuosos desempeñan un papel en la enfermedad.
Otros investigadores buscan posibles factores ambientales tales como las toxinas que pueden desencadenar el desorden y otros científicos están trabajando en la creación de nuevas medicinas protectoras que puedan retrasar, prevenir o revertir la enfermedad.
Desde el descubrimiento accidental de que el MPTP[1] ocasiona síntomas de Parkinson en los seres humanos, los científicos han encontrado que mediante la inyección de MPTP en animales de laboratorio, pueden reproducir las lesiones cerebrales que ocasionan estos síntomas.
Esto les permite estudiar los mecanismos de la enfermedad y les ayuda a crear nuevos tratamientos. Por ejemplo, fue de estudios con animales que los investigadores descubrieron que el medicamento selegilina puede prevenir los efectos tóxicos de MPTP.
Este descubrimiento ayudó a promover el interés en el estudio de la selegilina como tratamiento preventivo en los seres humanos.
Los científicos también están investigando el papel de las mitocondrias, estructuras en la célula que proporcionan energía para la actividad celular, en la enfermedad de Parkinson.
Debido a que el MPTP interfiere con el funcionamiento de las mitocondrias dentro de las células nerviosas, algunos científicos sospechan que algunas anormalidades similares pueden estar involucradas en la enfermedad de Parkinson.
Otras investigaciones en curso
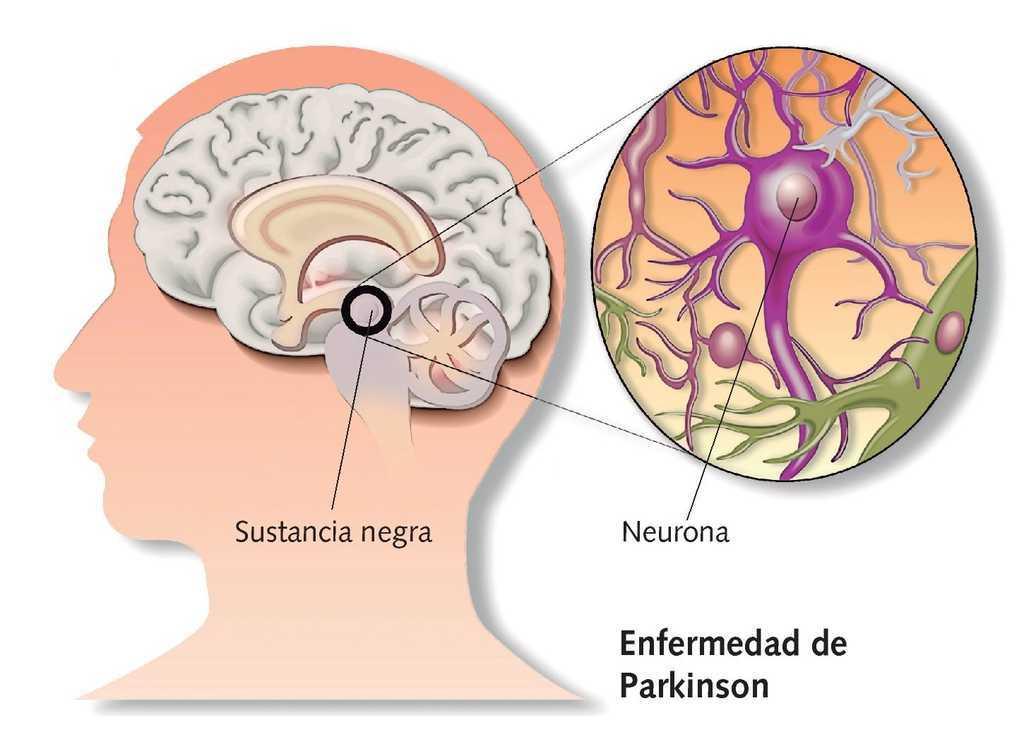
Actualmente hay prometedores estudios de áreas del cerebro distintas de la sustancia nigra que pueden desempeñar un papel en la enfermedad de Parkinson.
Un grupo de científicos apoyados por el Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares (NINDS, por sus siglas en inglés), estudia las consecuencias de la degeneración celular de dopamina en los ganglios basales – en la estructura del cerebro situada en un lugar profundo del prosencéfalo que ayuda a controlar el movimiento voluntario.
En animales de laboratorio, la reducción de dopamina inducida por MPTP resulta en sobreactividad de las células nerviosas en una región del cerebro denominada núcleo subtalámico, produciendo temblores y rigidez, lo que sugiere que estos síntomas pueden guardar relación con una actividad excesiva en esta región.
La destrucción del núcleo subtalámico resulta en una inversión de los síntomas de Parkinson en los modelos animales.
Los científicos apoyados por NINDS también buscan pistas sobre la causa de la enfermedad de Parkinson.
Para ello, estudian el mal funcionamiento de las estructuras llamadas «transportadores de dopamina» que conducen dopamina a y desde la sinapsis, o espacio estrecho entre las células nerviosas.
Por ejemplo, un grupo de investigación encontró una disminución relacionada con la edad en la concentración de transportadores de dopamina en células nerviosas humanas saludables, tomadas de áreas del cerebro dañadas por Parkinson.
Ello significa que cualquier amenaza para los transportadores de dopamina restante podría resultar en la enfermedad de Parkinson.
Avances en desarrollo de medicamentos
La investigación de medicamentos más eficaces contra la enfermedad de Parkinson probablemente se vea impulsada por el reciente aislamiento de al menos cinco receptores cerebrales individuales para dopamina.
La nueva información acerca de los efectos singulares de cada receptor de dopamina individual en áreas diferentes del cerebro ha llevado a nuevas teorías de tratamiento y ensayos clínicos.
Los científicos también estudian nuevos métodos para transmitir dopamina a áreas críticas del cerebro. Los investigadores apoyados por NINDS, utilizando un modelo animal de la enfermedad, implantaron diminutas partículas que contenían dopamina en regiones del cerebro afectadas por la enfermedad.
Precisa Carlos Muñoz Retana, que estos científicos, encontraron que dichos implantes pueden mejorar parcialmente los problemas de movimiento presentados por estos animales.
Los resultados de estos estudios indican que técnicas similares podrán algún día tal vez funcionar para las personas con la enfermedad de Parkinson.
Aunque la levodopa-carbidopa restaura el movimiento normal en las etapas iniciales del Parkinson, el tratamiento pierde su eficacia a medida que progresa la enfermedad (efecto de desaparición).
Un estudio reciente puso de manifiesto que con el medicamento experimental Ro 40-7592 cuando se añade al tratamiento medicamentoso estándar para la enfermedad de Parkinson, levodopa-carbidopa, la reducción de los síntomas se prolonga en más del 60%.
Los científicos de NINDS encontraron, que los pacientes tratados con levodopa- carbidopa y Ro 40-7592 experimentaron periodos más largos de mejoría en el movimiento.
Este nuevo y prometedor medicamento que bloquea la descomposición de la dopamina permitiría a los pacientes tomar dosis menores y cantidades más pequeñas de levodopa-carbidopa y reducir los problemas del efecto de desaparición. En la actualidad, Ro 40-7592 está aún en una etapa experimental.
También se están investigando fórmulas adicionales de liberación controlada de los medicamentos contra la enfermedad de Parkinson y bombas implantables que proporcionan un suministro continuo de levodopa para ayudar a los pacientes que tienen problemas con niveles fluctuantes de respuesta.

Los injertos e implantes
Otro método de tratamiento prometedor consiste en la implantación en el cerebro de cápsulas que contienen células productoras de dopamina. Las cápsulas se rodean de una membrana biológicamente inerte que permite pasar el medicamento a través de la membrana a una tasa cronometrada.
Los injertos neurales, o el transplante de células nerviosas, es una técnica experimental propuesta para el tratamiento de la enfermedad. Los investigadores apoyados por NINDS han demostrado en modelos animales que la implantación de tejido fetal de la sustancia nigra del cerebro al cerebro con la enfermedad de Parkinson ocasiona la regeneración de las células nerviosas dañadas.
NINDS otorgó una subvención para investigación a un grupo de científicos de tres instituciones para que realizasen un ensayo clínico controlado de implante de tejido fetal en seres humanos.
El tratamiento busca reemplazar las neuronas productoras de dopamina dañadas con neuronas fetales saludables, y mejorar así el movimiento y la respuesta a los medicamentos de los pacientes.
Un nuevo enfoque prometedor puede ser el uso de células genéticamente producidas -es decir, células que no provienen del sistema nervioso, tales como las de la piel, modificadas y producidas en un cultivo de tejidos- que podrían tener los mismos efectos beneficiosos.
[1] MPTP es un compuesto tóxico para el cerebro que provoca síntomas muy similares a los de la enfermedad de Parkinson, de ahí su empleo en la investigación científica.





0 comentarios